-
맥스웰-볼츠만 분포(Maxwell-Boltzmann Distribution)열역학 2024. 1. 20. 15:48
무수히 많은 입자들이 어떻게 거동할까? 입자 한개 한개의 움직임을 모두 계산하기에는 어려울 뿐만이 아니라 계산량이 매우 방대할 것이다. 이런경우 사용할 수 있는 모형 중에 하나가 확률 모형이다. 입자의 갯수가 적다면 주사위를 6번 던진다고 1~6이 모두 나오는 것이 아닌 것처럼, 확률에 기반한 설명은 잘 들어맞지 않겠지만, 기체의 운동처럼 입자가 아주 많은 경우라면 확률 모형은 현상을 잘 설명해준다. 이글은 이전에 고전역학적인 방법으로 맥스웰-볼츠만 분포를 유도해보았던 것을 정리하고자 작성하였다. 공업 수학에서 배우는 다변수 함수의 미적분과 고등학교 확률과 통계에서 배우는 내용이 익숙하다는 전제로 설명하겠다.
Prerequestion1- 가우스 적분
$$ \int_{-\infty}^{\infty} e^{-x^2} dx = \sqrt{\pi} $$
눌러서 증명 보기
먼저 주어진 함수를 회전시킨 함수 \(e^{-(x^2 + y^2)}\) 를 생각해보자
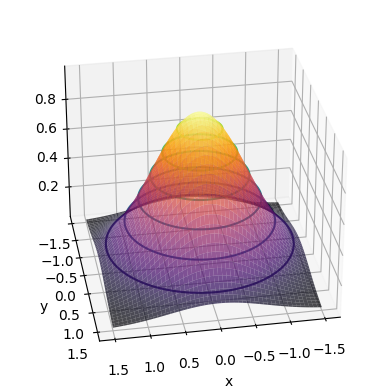
python matplot으로 그린 그래프 그럼 이 함수의 부피는 다음과 같은 이중 적분으로 구할 수 있다.
$$ \begin{align} V &= \int_{-\infty}^{\infty} e^{-(x^2 + y^2)} dx dy \\ &= \int_{-\infty}^{\infty} e^{-x^2} dx \int_{-\infty}^{\infty} e^{-y^2} dy\ (\textrm{Clairaut's rule}) \end{align} $$
여기서 \(x,\ y\)는 적분을 위한 더미 변수(형식적인 변수)이므로 \(y\)를 \(x\)로 바꾸어써도 문제 없다. 그러므로 식은 다음과 같이 정리된다.
$$ V = \left( \int_{-\infty}^{\infty} e^{-x^2} dx \right)^2 $$
그런데 회전체이므로 회전체의 부피를 구하는 방법으로도 부피를 구할 수 있다. 함수를 화장실 휴지처럼 수많은 shell로 나누어 부피를 구하면 다음과 같다.
$$\begin{align} V &= \int_0^{\infty} 2\pi x e^{-x^2} dx\\ &= \pi \int_0^{\infty} \dfrac{d}{dx} \left(-e^{-x^2}\right) dx\\ &= \pi \end{align}$$
두가지 방법으로 구한 부피는 같으니
$$ V = \left( \int_{-\infty}^{\infty} e^{-x^2} dx \right)^2 = \pi$$
$$ \therefore \int_{-\infty}^{\infty} e^{-x^2} dx = \sqrt{\pi} $$
증명 끝
Prerequestion2-확률과 통계
고등학교 수준의 확률과 통계 내용이다.
1점짜리 제비가 3개 2점 제비 2개, 3점 제비 1개가 있는 상자에서 뽑은 제비를 다시 상자에 넣어가면서 반복적으로 제비를 뽑는다고 해보자. 그럼 뽑은 사람의 점수 평균은 다음과 같이 구할 수 있을 것이다.
$$ \dfrac{ (\textrm{1 점}) \times (\textrm{뽑은 1점자리 제비 수}) +(\textrm{2 점}) \times (\textrm{뽑은 2점자리 제비 수}) + (\textrm{3 점}) \times (\textrm{뽑은 3점자리 제비 수}) }{(\textrm{시행 횟수})} $$
그럼 시행횟수가 무수히 많은 경우, 즉 이론적인 평균인 기대값은 어떻게 될까? (뽑은 1점 짜리 제비 수)/(시행 횟수)는 이론적인 확률인 (상자에 있는 1점 짜리 제비 수)/(전체 제비 수) = (1점 짜리 제비를 뽑을 확률)이 된다. 즉 이산확률분포를 따르는 확률 변수 \(X\)의 기대값은 다음과 같이 구할 수 있다.
$$ E(X) = \sum_i x_i p_i$$
여기서 \(x\)는 변수의 값, \(p\)는 해당 값이 나타날 확률이다. 만약 구간 \((a,b)\)에서 정의된 연속 확률 분포를 따른다면, 해당 분포의 확률 밀도 함수를 \(P\)라고 할 때 다음과 같이 기대값을 구한다.(연속 확률 분포에서는 그래프의 면적이 확률임을 유의)
$$ E(X) = \int_a^b xP(x) dx $$
Prerequestion3 - 라이프니츠 적분 규칙
이것 말고도 라이프니츠의 이름이 붙은 공식이 많으니 주의할 것
독립 변수 \(x,\ t\)에 대해서 어떤 열린 구간에서 정의된 연속이고 미분가능한 함수 \(f\)에 대해 다음 식이 성립한다.
$$\dfrac{d}{dt} \int_{a}^{b} f(x, t) dx = \int_{a}^{b} \dfrac{\partial}{\partial t}f(x, t) dx$$
연속이고 미분가능이라면, 서로 상관이 없는 변수(독립)의 미분과 적분 순서를 바꿀 수 있음을 의미한다.
눌러서 증명 보기
\(g(t)\)를 다음과 같이 정의하자(:=는 정의한다는 의미의 수학 기호이다.)
$$g(t) := \int_{a}^{b} f(x, t) dx $$
그럼 임의의 실수 t'에 대해 좌변의 식은 다음과 같다.
$$ \dfrac{d}{dt} g(t') = \dfrac{d}{dt} \int_{a}^{b} f(x, t') dx$$
연속이고, \(t\)에 대해서 미분가능한 함수이므로 평균값 정리를 적용하면, 임의의 실수 \(h\)와 열린구간 \((h, t')\)에 대해서 다음 식이 성립한다.
$$\begin{align} \dfrac{d}{dt} g(c) &= \dfrac{g(t' + h) - g(t')}{h} \\ &= \dfrac{ \int_{a}^{b} f(x, t' + h) dx - \int_{a}^{b} f(x, t') dx }{h}\\ &= \int_{a}^{b} \dfrac{f(x, t' + h) - f(x, t')}{h} dx \end{align} $$
여기서 \(h\rightarrow 0\)인 극한을 취한다면, \(c\rightarrow t'\)이 되고, 편미분의 정의에 따라서 아래와 같이 쓸 수 있다.
$$ \dfrac{d}{dt} g(t') = \int_{a}^{b} \dfrac{\partial}{\partial t}f(x, t') dx$$
이때 적분변수인 \(t'\)은 더미 변수(형식적인 변수)이므로 \(t\)로 바꾸어 쓰면 다음과 같이 된다.
$$\dfrac{d}{dt} \int_{a}^{b} f(x, t) dx = \int_{a}^{b} \dfrac{\partial}{\partial t}f(x, t) dx$$
증명 끝
Part A 열역학-에너지 등분배 정리
어떤 이론을 공부할 때, 그 이론에서 어떤 가정을 하였는 지 살펴보는 것이 중요한다. 어떤 가정을 하였는 지를 잘 알아야 상황에 맞게 적용할 수 있고, 가정에서 벗어난 상황이 닥쳤을 때, 상황에 맞춰 수식을 수정해볼 수도 있다. 가정한 상황과 달라서 잘 맞지 않는 것인데도 그냥 이론이랑 실험이 따로 논다고 생각하지 않았으면 좋겠다.
Assumption
- 이상기체(분자끼리 충돌하였을 때, 에너지가 보존(완전탄성충돌), 입자의 크기는 무시, 입자간의 힘 무시)
- 벽에 부딪혔을 때 입자의 에너지는 그대로 보존된다.
- 공간상의 \(x,\ y,\ z\) 방향은 서로 선형 독립(Linear Independent)이며, 등방적(Isotropic)이다.
- 입자는 고전적인 물리법칙에 따라 운동한다.
- 기체는 열역학적 평형을 이룬 상태이다.(온도가 일정한 상태이다.)
우리가 눈으로 보는 거시 세계에서는 충돌한다고 완전탄성충돌이 일어나지는 않고, 입자끼리의 전자기적 상호작용 등으로 인해 일부가 물체를 이루는 입자의 진동 에너지 형태 즉 열로 손실된다. 그러나 미시세계에서는 그러한 입자끼리 충돌을 하는 것으로 열로 손실되거나 하지 않는다.(입자의 평균 운동에너지가 열이라는 점을 상기하면 된다.) 만약에 충돌로 인해 에너지가 손실된다면 점점 기체 분자들이 에너지를 잃어가다 정지하게 되는데, 이 지점은 절대 영도로써 불가능하다고 알려져있기 때문이다. 또한 정전기력같은 입자간의 힘이 무시되므로 이상기체의 에너지는 운동에너지만 고려하면 된다.
그럼이제 한 변의 길이가 \(d\)인 정육면체 내부에 이상기체 입자가 운동한다고 생각을 해보자. (많은 입자들이 이 안에 있겠지만, 생략하고 1개만 그렸다.) 그림에 있는 입자는 주변 이상기체 입자들과 충돌하기 때문에 이 정육면체 영역에서만 운동하게 된다. \(x,\ y,\ z\) 방향이 독립이며, 등방적이므로 \(x\)방향의 운동만 고려하면 된다.

\(x\)성분만 본다면, 입자는 한쪽 벽과 맞은 편 벽을 일자로 왔다갔다하는 상황과 같으며, 평균적으로 \(\Delta t\)의 시간동안 입자는 한쪽벽에 부딪혔다. 다른쪽 벽에 부딪혀 \(2d\)의 거리를 움직이게 된다. 따라서 입자의 평균 속력은 아래와 같이 쓸 수 있다.
$$\bar{v}_x= \dfrac{2d}{\Delta t}$$
그리고 입자가 한쪽벽에 튕겨서 다시 원래 자리로 돌아오는 상황에서 운동량의 평균적이 변화량은 \(-2mv\)가 되며, 충돌시간은 \(\Delta t\)가 된다.(우리가 보는 거시세계라면 왔다갔다하는 시간에 비해 충돌 시간은 매우 짧으므로, 충돌시간은 \(\Delta t\)도, \(\frac{\Delta t}{2}\)도 아니다. 그러나 \(d\)가 아주 작아서, 왼쪽벽과 오른쪽 벽이 거의 맞닺아있는 상태라 생각을 해보자. 왔다갔다 하는 시간과 충돌시간은 차이가 나지 않게된다.) 따라서 입자가 받은 충격량의 크기는 운동량과 충격량 사이의 관계에 따라 \(2mv\)가 되며, 충격량의 정의를 이용하면 평균힘의 크기를 다음과 같이 알 수 있다.
$$\begin{align} \mathbf{I} &:= \mathbf{ \bar{ F}}_{\textrm{평균}} \cdot \Delta t \\ &= \Delta p \end{align}$$
$$ \mathbf{ \bar{ F}}_{x} \cdot \dfrac{2d}{ \bar{v}_x } = 2m \bar{v}_x $$
$$ \mathbf{ \bar{ F}}_{x} = \dfrac{m {\bar{v}_x}^2}{d} $$
또한 \(N\)개의 입자가 벽을 두드리면서 압력을 형성하는 것이므로, 압력은 다음과 같이 쓸 수 있다.
$$ P_x = \dfrac{\Sigma \mathbf{ \bar{ F}}_{x} }{d^2} = N\dfrac{m {\bar{v}_x}^2}{d^3} $$
입자가 운동하는 영역의 부피는
$$ V = d^3 $$
마지막으로 이상기체 상태방정식 \(PV=nRT\)에서
$$ R = \dfrac{k_b}{N_a}\\\ (k_b:\text{볼츠만 상수},\ N_a:\text{아보가드로수})$$
인 관계가 있으므로 다음과 같이 쓸 수 있다.(물리에서 많이 사용사용하는 형태)
$$ PV = Nk_b T$$
이때 우리가 구한 것은 \(x\) 방향에 대한 압력이고, 이상기체 방정식은 \(x,\ y,\ z\)방향이 모두 고려된 압력이다. 따라서 이를 맞춰줄 필요가 있다. 각 공간의 각 성분이 선형 독립이라 가정하였으므로 다음과 같이 압력은 각 성분에 대한 선형 결합으로 표현된다.
$$ P = P_x + P_y + P_z $$
이는 각 성분별로 따로 구한 뒤 더할 수 있다는 말이다. 먼저 우리가 구한 \(x\)성분만 먼저 대입해보면 다음과 같다.
$$ m{\bar{v}_x}^2 = k_b T$$
$$ \dfrac{1}{2}m{\bar{v}_x}^2 = \dfrac{1}{2}k_b T$$
여기에 등방적이라 가정하였으므로 나머지 성분에 대한 결과 역시 같다.
$$ \dfrac{1}{2}m{\bar{v}_y}^2 = \dfrac{1}{2}k_b T$$
$$ \dfrac{1}{2}m{\bar{v}_z}^2 = \dfrac{1}{2}k_b T$$
각 식을 더해보면 다음과 같다.
$$ \dfrac{1}{2}m( {\bar{v}_x }^2 +{\bar{v}_y }^2 +{\bar{v}_z }^2 ) = \dfrac{3}{2}k_b T$$
3차원 공간상에서 속력은 다음과 같이 쓸 수 있다.
$$ \bar{v} = \sqrt{{ \bar{v}_x }^2 + {\bar{v}_y }^2 + {\bar{v}_z }^2 } $$
정리하면 다음과 같이 이상기체 입자 1개당 평균 운동에너지와 온도의 관계를 알 수 있다.(입자수를 나타내는 \(N\)이 양변에서 소거 되었으므로)
$$ \dfrac{1}{2}m {\bar{v} }^2 = \dfrac{3}{2}k_b T$$
이 식이 말해주는 것은 온도는 미시적인 입자의 평균 운동에너지라는 것이다.
에너지 등분배법칙(Energy Equipartitions Law)
앞에서는 입자를 하나의 점으로 간주하였으므로, \(x, y, z\) 세 방향의 운동만 고려하였다. 이 식은 18족 비활성기체에 대해서는 잘 맞아떨어지나, 산소 분자, 질소 분자등은 잘 맞지 않는다. 왜냐하면 이들 분자는 구성하는 원자가 진동이나 회전을 할 수 있기 때문이다. 진동을 표현하는데 2개의 성분이 더 필요하고, 회전을 표현하는데도 2개의 성분이 더 필요하다. 이러한 성분의 숫자를 자유도(degree of freedom)라고 부르며, \(x,\ y,\ z\) 세 방향의 운동만 한다면 자유도 3인 운동을, 여기에 회전과 진동을 더 한다면 자유도는 3+2+2=7이 되는 것이다. 위의 유도 과정에서 \(x,\ y,\ z\) 성분 각각 \(\frac{1}{2}k_b T\)의 에너지를 똑같이 가졌는데, 회전과 진동역시 자유도 1당 \(\frac{1}{2}k_b T\)의 에너지를 가진다. 즉 열역학적 평형상태에서는 자유도 1당 \(\frac{1}{2}k_b T \)의 에너지를 가진다고 할 수 있는데 이를 에너지 등분배법칙(Energy Equipartitions Law)이라 한다.
Part B 통계역학-맥스웰 볼츠만 분포(속력)
열역학적 평형 상태에서 자유도가 3이고, \(x,\ y,\ z\) 방향이 선형 독립이며, 등방적인 운동을 하는 이상 기체를 가정해보자. 세 방향의 속도 \(v_x,\ v_y,\ v_z\)에 대해서, 등방적이므로 각 확률분포는 \(g(v_x),\ g_(v_y),\ g(v_z)\)가 된다. 또한 세 방향이 선형독립이므로, 확률적으로도 독립인 사건이 되어 특정 \(v_x,\ v_y,\ v_z\)은 확률의 성질에 따라 \(g(v_x) \times g_(v_y) \times g(v_z)\)가 된다. 이때 이 함수는 등방적이어야 하므로 구대칭이어야 한다. 쉽게 말해 속도가 \(<1, 2, 3>\)일 확률이나 \(<2, 1, 3>,\ <2, 3, 1>,\ <1, 3, 2>,\ <3, 1, 2>,\ <3, 2, 1>,\ <-1, 2, 3>, \cdots \)일 확률, 즉 같은 속력에 대해선 \(g(v_x), g(v_y), g(v_z)\)의 곱이 동일해야한다는 것이다. 이를 수학적으로 표현하면 다음과 같다.
$$ G( {v_x }^2 + {v_y }^2 + {v_z }^2 ) = g(v_x) g(v_y) g(v_z) $$
여기서 \(G\)는 속력의 제곱을 입력받아 확률값을 반환하는 함수가 된다. 직관적으로 지수함수 형태가 위 식을 만족시킨다는 것을 알 수 있다.
$$ e^{ {v_x }^2 + {v_y }^2 + {v_z }^2 } = e^{{v_x}^2} \times e^{{v_y}^2} \times e^{{v_z}^2} $$
조금 더 일반적으로 아래 형태의 지수함수 역시 주어진 식을 만족한다.
$$ ae^{bx} $$
이때 확률분포는 모든 정의역에 대해 적분하였을 때 1이 나와야하므로 양수 \(A,\ B\)에 대해서 함수 \(g\)는 다음과 같은 형태임을 알 수 있다. (-가 붙지 않으면, 발산하기 때문)
$$ g(v_x) = Ae^{-B{v_x}^2} $$
\(v_y,\ v_z\)에 대한 확률 분포 역시 \(g\)이므로 \(G\)는 아래와 같이 쓸 수 있다.
$$ G({v_x }^2 + {v_y }^2 + {v_z }^2 ) = A^3 e^{-B({v_x }^2 + {v_y }^2 + {v_z }^2 )} $$
여기서 G는 확률 밀도 함수의 성질을 가지고 있지만, 속력의 제곱에 대한 함수이므로 이를 속력에 대한 함수로 변환해주어야 한다. 저 식을 구면 좌표에서 나타낸다면 속도를 속력을 매개변수로하여 표현할 수 있으니 속력에 대한 분포를 얻기 위해서는 구면 좌표로 바꾸어줄 필요가 있다.
속력에 대한 분포를 \(f(v)\)라 하자. 확률 분포의 정의역을 모두 적분한다면 1이 나와야하므로 다음 식이 성립해야한다.
$$ \int_0^{\infty} f(v) dv = \int_{-\infty}^{\infty} \int_{-\infty}^{\infty} \int_{-\infty}^{\infty} G({v_x }^2 + {v_y }^2 + {v_z }^2 ) d{v_x} d{v_y} d{v_z} = 1 $$
직교좌표계에서 구면좌표계로 식을 변환하면
$$ d{v_x} d{v_y} d{v_z} = v^2 \sin{\phi} dv d\phi d\theta$$
$$ 0 \leq v \leq \infty,\ 0 \leq \phi \leq \pi,\ 0 \leq \theta \leq 2\pi $$
이므로
$$ \begin{align} \int_0^{\infty} f(v) dv &= \int_{0}^{2\pi} \int_{0}^{\pi} \int_{0}^{\infty} A^3 v^2 \sin{\phi}e^{-Bv^2} dv d\phi d\theta \\ &= \int_{0}^{2\pi} d\theta \int_{0}^{\pi} \sin{\phi} d\phi \int_{0}^{\infty} A^3 v^2 e^{-Bv^2} dv\ (\textrm{Clairaut's rule})\\ &= \int_{0}^{\infty} 4\pi A^3 v^2 e^{-Bv^2} dv \end{align} $$
좌우변을 비교해보면 아래와 같음을 알 수 있다.
$$ \therefore f(v) = 4\pi A^3 v^2 e^{-Bv^2} $$
이제 미지수가 2개 이므로, 2개의 식이 필요하다. 세제곱이 있어 불편하므로 편의상 \(C = 4\pi A^3\)으로 두고 \(C\)와 \(B\)를 찾자
확률 분포의 규격화
첫번째로 앞에서도 언급하였듯 모든 경우의 수에 대해서 일어날 확률은 1이기 때문에 확률 밀도 함수의 정의역을 모두 적분한다면 1이 나와야한다. \(f(v)\)를 가지고 적분하기는 어려우니 적분하기 쉬운 \(g(v_x)\)가지고 \(A,\ B\) 사이의 관계식을 구해보자(\(g\)는 속도에 대한 확률분포라고 하였으므로, \(f\)와 마찬가지로 적분해서 1이 된다는 조건을 만족해야 한다. (참고로 \(G\)는 속력이 아닌 속력의 제곱이 입력값으로 들어가는 함수이므로, \(G\)를 이용해선 안된다. \(G\)를 규격화하여 \(A,\ B\)의 관계식을 찾으면, \(g\)는 규격화가 안되는 문제가 발생한다.)
$$ g(v_x) = Ae^{-B{v_x}^2} $$
$$ \int_0^{\infty} Ae^{-B{v_x}^2} dv = 1 $$
가우스 적분은 다음과 같다.
$$ \int_{-\infty}^{\infty} e^{-x^2} dx = \sqrt{\pi} $$
그러므로 다음과 같다.
$$ A\dfrac{ \sqrt{\pi} }{\sqrt{B}} = 1 $$
$$ A = \sqrt{ \dfrac{B}{\pi} } $$
$$\therefore C = 4\pi A^3 = 4\sqrt{\dfrac{B^3}{\pi} }$$
열역학
앞서 에너지등분배 법칙에서 자유도가 \(\alpha\)인 이상기체는 다음과 같은 식이 성립한다고 하였다.
$$ \dfrac{1}{2}m \bar{v}^2 = \dfrac{\alpha}{2}k_b T $$
또한 하나의 점으로 간주하고 있으므로 자유도는 3이 된다. 그러므로 기체 분자의 평균 제곱 속력은 다음과 같다.
$$ \bar{v}^2 = \dfrac{3k_b T}{m}$$
그리고 평균 제곱 속력은 확률 분포를 이용해서도 다음과 같이 구할 수 있다.
$$ \begin{align} \bar{v}^2 &= \int_0^{\infty} v^2 f(v) dv\\ &= C \int_0^{\infty} v^4 e^{-Bv^2} \end{align} $$
해당 적분은 다음 방법으로 계산할 수 있다. 먼저 가우스 적분에서
$$ \int_0^{\infty} e^{-Bv^2} dv = \dfrac{ \sqrt{\pi} }{2} B^{-\frac{1}{2} } $$
이 함수를 \(B,\ v\)에 대한 이변수 함수로 보고 양변을 \(B\)에 대해서 2번 미분하면 된다. 이때 함수가 균등 수렴(uniform convergence)하니 미분이 극한안으로 들어갈 수 있으며, 연속이고 미분가능한 함수이므로 라이프니츠 적분 규칙에 따라 미분이 인테그랄 안으로 들어갈 수 있다.
$$ \int_0^{\infty} -v^2 e^{-Bv^2} dv = -\dfrac{ \sqrt{\pi} }{4} B^{-\frac{3}{2} } $$
$$ \int_0^{\infty} v^4 e^{-Bv^2} dv = \dfrac{ 3\sqrt{\pi} }{8} B^{-\frac{5}{2} } $$
위 결과를 모두 종합하면 다음의 식이 나온다.
$$ \bar{v}^2 = \dfrac{3k_b T}{m} = C \dfrac{ 3\sqrt{\pi} }{8} B^{-\frac{5}{2} }$$
\(C\)를 대입해서 정리하면 다음과 같다.
$$ \dfrac{k_b T}{m} = 4\sqrt{\dfrac{B^3}{\pi}} \times \dfrac{\sqrt{\pi}}{8} B^{-\frac{5}{2}} $$
$$ \dfrac{k_b T}{m} = \dfrac{1}{2B} $$
$$ \therefore B = \dfrac{m}{2k_b T} $$
$$ C= \dfrac{4}{\sqrt{\pi}}B^{ \frac{3}{2} } = \dfrac{4}{\sqrt{\pi}}{\left( \dfrac{m}{2k_b T} \right)}^{ \frac{3}{2} } = 4\pi {\left( \dfrac{m}{2\pi k_b T} \right)}^{ \frac{3}{2} } $$
그러므로 맥스웰 볼츠만 분포는 다음과 같다.
$$ f(v) = 4\pi {\left( \dfrac{m}{2\pi k_b T} \right)}^{ \frac{3}{2} } v^2 e^{-\dfrac{m}{2k_b T}v^2} $$
그리고 화학에서는 다음의 관계를 이용해 몰질량 \(M\)과 이상기체 상수 \(R\)로 맥스웰 볼츠만 분포를 나타낸다.
$$ M = N_a m, R = N_a k_b $$
$$ f(v) = 4\pi {\left( \dfrac{M}{2\pi RT} \right)}^{ \frac{3}{2} } v^2 e^{-\dfrac{M}{2RT}v^2} $$
이때 주의해야할 점은 식이 MKS 단위계이기 때문에 분자량의 단위를 kg/mol로 해야하며, 이상기체상수의 단위 역시 J/(K·mol)로 해야한다.
rms 속도는 유도 과정에서 등장하였으며, 최빈 (most probable) 속도는 그래프를 미분하여 극점을 찾는 것으로, 평균 속도는 \(v\)를 곱하여 적분하여 구할 수 있다.
$$ v_{\mathrm{mp}} = \sqrt{ \dfrac{2k_b T}{m} }$$
$$ v_{\mathrm{avg}} = \sqrt{ \dfrac{8 k_b T}{\pi m} } $$
$$ v_{\mathrm{rms}} = \sqrt{ \dfrac{3k_b T}{m} } $$
유도 과정 보기
계산 편의상 다시 \(C,\ B\)로 치환하여 계산하자
최빈 속도
$$ \begin{align} f'(v) &= 2Cv e^{-Bv^2} + Cv^2 \left( -2Bv e^{-Bv^2} \right)\\ &= 2Cv e^{-Bv^2} \left( 1 - Bv^2 \right) \end{align} $$
$$ v_{\mathrm{mp}} = \sqrt{ \dfrac{1}{B} } = \sqrt{ \dfrac{2k_b T}{m} } $$
평균 속도
부분적분 두 번 해주면 된다.
$$\begin{align} v_{\mathrm{avg}} &= \int_0^{\infty} Cv^3 e^{-Bv^2} dv\\ &= -\dfrac{C}{2B} \int_0^{\infty} v^2 \dfrac{d}{dv}\left( e^{-Bv^2} \right) dv\\ &= -\dfrac{C}{2B} \int_0^{\infty} -2Bv e^{-Bv^2} dv\\ &= \dfrac{C}{2B^2}\\ &= \dfrac{2}{\sqrt{\pi}}B^{-\frac{1}{2}}\\ &= \sqrt{ \dfrac{8k_b T}{\pi m} } \end{align}$$
RMS 속도
에너지 등분배법칙에서 (\(v^2\)을 곱해서 적분해도 되지만, 유도과정에서 이미 하였을 뿐더러 귀찮다)
$$ \dfrac{1}{2}m v_{\mathrm{rms}}^2 = \dfrac{3}{2}k_b T $$
$$ v_{\mathrm{rms}} = \sqrt{ \dfrac{3k_b T}{m} } $$
증명 끝
맥스웰 볼츠만 분포 그래프
질소의 원자량은 14 정도이다. (Nitrogen, Wikipedia, https://en.wikipedia.org/wiki/Nitrogen) 그러므로 질소 분자의 몰질량은 28 g/mol이며 이를 kg으로 환산하면 다음과 같다.
$$ M = 0.028\ \mathrm{kg/mol}$$
다음으로 0 ˚C, 1 atm에서 1 mol의 기체 분자는 22.4 L의 부피를 차지한다는 사실을 이용해서 기체 상수를 구할 수 있는데, 모두 SI 단위로 변경해주어야 한다. 0 ˚C는 273.15 K이며, 1 atm = 101325 Pa이다. 그리고 \(1\ \mathrm{ml} = 1\ \mathrm{cm^3}\) 이므로 \(1\ \mathrm{L} = 10^{-3}\ \mathrm{m^3}\)이다.
$$ R = \dfrac{101325\ \mathrm{Pa} \times 22.4 \times 10^{-3}\ \mathrm{m^3} }{1\ \mathrm{mol} \times 273.15\ \mathrm{K}} = 8.31\ \mathrm{J\cdot K^{-1} \cdot mol^{-1} }$$
import math import numpy as np import matplotlib.pyplot as plt R = 101325 * 22.4*1.E-3 / (1*273.15) M = 28.02/1000 v = np.linspace(0, 2500, 10000) f = lambda T : 4*math.pi * (M/(2*math.pi*R*T))**(3/2) * v**2 * np.exp(-M/(2*R*T)*v**2) plt.figure(dpi=130) plt.title("Maxwell-Boltzmann Distribution ($N_2$)") plt.xlabel("Speed (m/s)") plt.ylabel("Probability Density") plt.plot(v, f(273.15), label="273.15 k", color="#4587ef") plt.plot(v, f(293.15), label="298.15 k", color="#ff9e47") plt.plot(v, f(1000), label="1000 k", color="#ff2e47") plt.legend() plt.show()
결론
맥스웰 볼츠만 분포는 계의 미시적인 입자들이 어떻게 움직이는 지를 알려준다. 유도한 식을 변형하여 속도나 에너지에 대한 분포를 얻을 수도 있으며, 충돌 이론에서는 활성화 에너지 이상을 가진 입자가 충돌할 확률을 맥스웰 볼츠만 분포를 확용하여 구한다. 개인적으로 한 번, 화학 보고서 적으면서 또 한 번 유도해보았기에 여기에 금방 정리할 수 있을 것이라 생각을 하였지만, 티스토리에서 수식을 적는 게 불편해서 생각보다 정리하는데 오래걸렸다.(기본 편집기에서 수식을 복붙하면 html로 확인하였을 때 필요없는 문자까지 붙여넣기가 되어 오류가 생긴다. 그래서 html로 일일히 이를 다시 확인하느라 시간을 많이 잡아먹었다.)
혹시 잘못 설명한 부분이 있다면 댓글로 알려주시면 감사하겠습니다.
참고 문헌
Raymond A. Serway, John W. Jewett, 『 Physics for Scientists and Engineers with Modern Physics』, Cengage Learning (2018)
History
2024.03.15 몰질량과 볼츠만 상수에 관한 오타 수정, 유도 과정안의 표현도 조금 수정
'열역학' 카테고리의 다른 글
[열역학] 4. 화학 포텐셜(Chemical Potential)과 평형(Equilibrium), 르 샤틀리에 원리(Le Chatelier's Principle)의 열역학적 근거 (2) 2024.07.13 [열역학] 3. 자유 에너지와 맥스웰 관계식(Maxwell Relation) (0) 2024.07.13 [열역학] 2. 카르노 기관(Carnot Engine)과 열역학 제 2 법칙 (3) 2024.07.11 [열역학] 1.열역학 제 1 법칙과 내부 에너지(Internal Energy), 엔탈피(Enthalpy) (1) 2024.07.10 [열역학] 열역학의 공리와 기본 개념 (2) 2024.07.10